이번 연구 결과는 암 연구 분야의 세계적 권위지인 Cancer Communications (IF: 24.9, JCR 상위 3.5%)에 “DKK1 Suppresses Hippo Signaling via PIP3–OGT–LRP6 O-GlcNAcylation in Hepatocellular Carcinoma”라는 제목으로 게재되었다.
연구팀은 간암에서 과발현되는 분비 단백질인 “DKK1”이 암세포의 비정상적인 증식과 전이를 유도하는 상세한 분자 기전을 규명했다. 기존 연구들이 DKK1에 의한 단순 PIP3 형성에 주목했다면, 이번 연구는 수용체 단백질인 “LRP6”의 독특한 번역 후 변형(Post-translational modification)인 “O-GlcNAcylation”이 DKK1 유래 암세포 성장의 핵심 분자기전임을 세계 최초로 증명했다.
DKK1에 의해 유도된 LRP6의 O-GlcNAcylation은 간암 조직 내에서 암 억제 신호인 “Hippo 신호전달”을 차단하고, 결과적으로 발암 단백질인 “YAP”을 활성화해 암세포의 생존과 전이 능력을 폭발적으로 증가시킨다는 사실을 확인했다.
연구팀은 이러한 발암 과정을 차단하기 위해 ‘PPO (PIP3-binding domain of OGT)’ 도메인을 활용한 혁신적인 ‘PIP3 masking’ 전략을 제시했다.
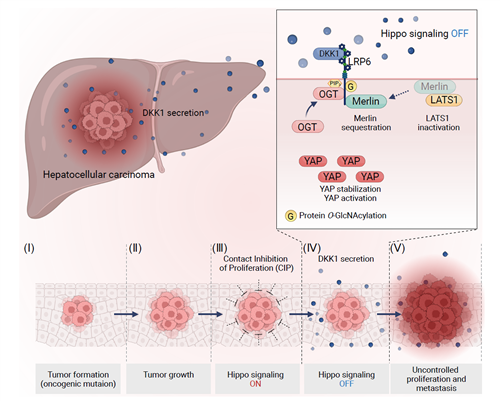
기존의 O-GlcNAcylation 억제제는 암세포뿐만 아니라 정상 세포의 대사까지 저해해 부작용 우려가 컸다. 그러나 연구팀이 개발한 PPO 전략은 세포막이라는 국소 부위에서만 선택적으로 작용한다. 이를 통해 세포막으로 이동하는 OGT 단백질을 차단하고 LRP6의 변형을 막음으로써, Hippo 신호전달을 재활성화하고 YAP 단백질을 효과적으로 억제하는 데 성공했다.
특히, 이 전략은 DKK1 발현이 높은 간암뿐만 아니라, 다양한 암종에서 공통으로 나타나는 PIP3 증가 상황에서도 범용적인 항암 효과를 보였다. 반면, DKK1이나 PIP3 형성이 적은 정상 세포에서는 영향이 거의 확인되지 않아 암 특이적인 정밀 치료 가능성을 입증했다.
조익훈 교수는 “이번 연구는 치료제가 마땅치 않은 진행성 간암 환자들에게 새로운 희망이 될 수 있는 치료 전략을 제시했다는 데 큰 의미가 있다”며, “PPO 전략은 다양한 암종에 적용 가능한 범용성을 갖추고 있어, 향후 DKK1 발현 수치를 기반으로 한 환자 맞춤형 정밀 항암 치료 플랫폼으로 발전시킬 수 있을 것”이라고 밝혔다.
한편 이번 연구는 한국연구재단(NRF), BK21 사업 등의 지원을 받아 수행되었다.
이번 성과는 탄탄한 분자기전을 기반으로 새로운 항암전략을 제시한 연구로, 정상 세포의 부작용은 최소화하고 치료 효능은 극대화함으로써, 환자 맞춤형 정밀 의료와 범용 항암제 개발의 중요한 토대를 마련한 것으로 평가된다.
[ⓒ 대학저널. 무단전재-재배포 금지]